CAR T細胞療法の世界市場:製品別(イエスカルタ(アキシカブタゲン・シロルユーセル))市場予測2024年~2031年

※本ページに記載されている内容は英文レポートの概要と目次を日本語に自動翻訳したものです。英文レポートの情報と購入方法はお問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
CAR T-Cell Therapy Market by Product (Yescarta (axicabtagene ciloleucel), Kymriah (tisagenlecleucel), JCAR017 (lisocabtagene maraleucel), bb2121), Indication (Relapsed Large B-cell Lymphoma, Acute Lymphoblastic Leukemia (ALL), Multiple Myeloma), End User (Car T-Cell Therapy at Hospitals, Car T-Cell Therapy at Cancer Treatment Centers), and Regional Analysis from 2024 to 2031
CAR T細胞療法市場の規模とシェア分析
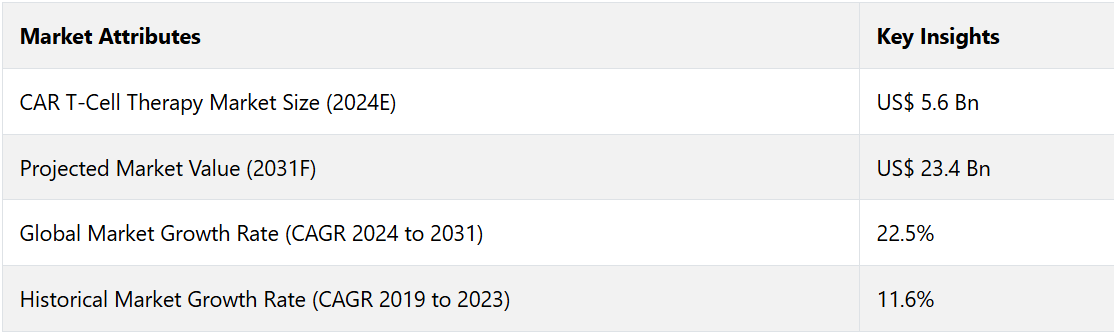
世界のCAR T細胞療法市場は、2024年から2031年の予測期間にわたって、年平均成長率(CAGR)22.5%で成長すると予測されています。2024年に記録された56億米ドルから、2031年には234億米ドルに増加すると予測されています。
業界の拡大は、大手企業の存在、研究開発への投資、政府からの資金援助によって後押しされています。がん罹患率の上昇と革新的な治療法の登場により、CAR T細胞に対する需要はさらに高まっています。
2000年から2021年の間に、がんの新規症例数は36.3%増加し、年間診断数は約130万件から180万件に増加しました。この数値は、がん罹患率の著しい上昇を示しています。米国がん協会の予測によると、2024年に米国では初めてがんの新規症例が200万件を超えると見込まれており、がん診断の増加が続いていることを示しています。患者数の増加に伴い、消費者はCAR T細胞療法を採用する可能性が高く、産業用プレーヤーの道筋が生まれています。
市場の主なハイライト
- 2024年には、北米が市場の66.9%のシェアを占める見通しです。
- 2024年には、北米における価値シェアの98.8%以上を米国が占める見通しです。
- 2031年までに、アジア太平洋地域が市場で著しく成長する地域になると予測されています。
- 政府による強力な支援と患者数の増加が、産業用成長の主な要因となっています。
- 製品別では、イエスカルタ(アキシカブタゲン・シロルユーセル)がその有効性を反映して、2024年には市場シェアの57.8%以上を占めることが予測されています。
- 適応症別では、再発性大B細胞リンパ腫がCAR T細胞療法市場の約90.7%を占めることが予測されています。
- がん患者数の増加に伴い、CAR T細胞の需要も大幅に増加すると予測されています。
- 大手ライフサイエンス企業は、CAR T細胞療法の製造にますます投資しており、FDAによる治療法の承認も進んでいます。
北米のCAR T細胞療法市場は、主要企業の存在により勢いを増している
北米は2024年には市場の66.9%のシェアを維持すると予測されている。この強力な地位は、主要企業の存在、政府による資金援助の増加、活発な研究努力によって支えられている。包括的な保険適用が、この地域が産業用で優位を占めることに貢献している。
2024年には、北米CAR T細胞療法市場における米国の金額シェアは98.8%を超えると予測される。米国では、CAR T細胞の開発・製造に注力するライフサイエンス企業が増加していること、また、同地域における品質管理システムの強化により、需要が拡大している。例えば、
米国に拠点を置く企業であるBoomiは、2024年10月にコネクターを発売しました。このデバイスは、サードパーティシステムとVeeva Vaultプラットフォーム間の統合を提供し、ライフサイエンスデータ共有におけるVeeva Systemsとの連携を強化します。
アジア太平洋CAR T細胞療法市場は、政府の強力な支援によりリードする
アジア太平洋地域は、2031年までにCAR T細胞療法において著しい成長が見込まれる地域です。2024年から2031年にかけて、年平均成長率(CAGR)27.94%で拡大すると予測されています。この急速な拡大は、患者数の増加と、製品および市場参加者を対象とした政府の強力な支援によって推進されています。
大手企業は先進的な治療法の開発にますます重点を置いており、市場の成長をさらに後押ししています。例えば、中国国家医薬品監督管理局(NMPA)は、再発または難治性のマントル細胞リンパ腫の成人患者を対象としたJWセラピューティクスの「カーティバ」の生物製剤追加承認申請を承認しました。この追加承認は、中国の臨床試験でも裏付けられています。
また、臨床試験の増加も産業の拡大に貢献しています。臨床試験データベース2023によると、現在、中国では約103件のCAR T療法が活発に臨床試験が行われています。
優れた性能と効果で市場をリードするイエスカルタ(アキシカブタゲン・シロルユーセル)
CAR T細胞療法イエスカルタ(アキシカブタゲン・シロルユーセル)の大規模ランダム化第3相臨床試験では、侵攻性非ホジキンリンパ腫(NHL)の一部の患者に治癒効果があることが分かっています。米国臨床腫瘍学会(ASCO)の年次総会で発表されたこの研究では、axi-celの投与を受けた患者の55%が4年後も生存しているのに対し、再発性疾患に対する標準治療を当初から受けた患者の46%が4年後も生存していると推定されています。 この結果から、axi-celは、びまん性大細胞型B細胞リンパ腫が急速に再発したり、標準的な初期治療に抵抗性を示したりする患者にとって、現在、最も望ましい治療法であることが示唆されています。
再発性大細胞型B細胞リンパ腫への投資拡大ががん治療への希望を示す
適応症別では、再発性大B細胞リンパ腫が2024年の市場シェアの約90.7%を占める見通しです。この高い市場シェアは、この難治性のリンパ腫の管理に有効な治療法が強く求められていることを示しています。なぜなら、患者はがんが再発したり改善が見られなかったりすると、限られた治療選択肢に苦慮することが多いからです。
さまざまな企業や組織が、大B細胞リンパ腫とその治療法の研究と理解に投資しています。例えば、米国の製薬・バイオテクノロジー企業であるファイザー社の第3相臨床試験「ECHELON-3」では、ADCETRISをレナリドミドおよびリツキシマブと併用することで、プラセボと比較して患者の死亡リスクが37%減少することが明らかになりました。この試験結果は、がん治療に新たな希望をもたらすものです。
市場導入と傾向分析
CAR T細胞療法は、患者のT細胞を改変することで癌と闘うことを目的とした革新的な治療法です。これは、より広義のT細胞療法の市場シェアの約27.1%を占めています。
がんの罹患率が上昇し続けているため、CAR T細胞に対する需要は大幅に増加すると予想されています。米国では、2000年から2021年にかけて、全国的な新規がん患者数は36.3%近く増加しました。同国では、がん関連死が約611,000件に達すると予想されており、これは毎日1,600人以上ががんで死亡していることを意味します。がんの罹患率が増加していることは、CAR T細胞療法のような効果的な診断法が急務であることを示しています。
がん治療にキメラ抗原受容体を使用することに焦点を当てた、ライフサイエンスおよびバイオテクノロジー分野における研究開発が著しく増加しています。CAR T細胞療法の有効性を確認するための研究が世界中で実施されています。このアプローチにより、主に白血病やリンパ腫と闘う患者を対象に、その有効性、メカニズム、患者コンプライアンスに関する理解が深まるでしょう。
歴史的な成長と今後の見通し
CAR T細胞療法市場は、2019年から2023年の期間に著しく成長しました。がん治療におけるCAR T細胞療法の使用増加は、依然として市場成長の主な要因となっています。
米国におけるがん患者数の増加が市場を牽引しています。このプロセスには、患者からT細胞を抽出し、高度な製造施設に送ってさらに処理することが含まれます。現在、CAR T細胞を製造している施設は、米国と欧州に数か所しかない。
細胞ベースの治療に対する需要の高まりを受け、複数のメーカーがCAR T細胞の製造に投資している。2017年にCAR T細胞療法が承認されると、大手ライフサイエンス企業がCAR T細胞製品の製造を開始した。複数の企業が政府から承認を受け、市場に製品を提供している。例えば、
- 米国の製薬会社であるブリストル・マイヤーズスクイブ社は、BreyanziについてFDAの承認を取得しています。これは、T細胞療法に使用されるCD19標的キメラ抗原受容体です。この受容体は、再発性または慢性リンパ性白血病の成人患者を治療することができます。
CAR T細胞療法市場の拡大は今後数年間も続くと予想されています。2031年までの年間平均成長率(CAGR)は22.5%に達すると見込まれています。CAR T細胞の臨床試験数の増加、製造における主要産業用プレーヤー、効果的な癌治療に対するニーズの高まりが、この成長を後押ししています。
市場成長の推進要因
CAR T細胞療法の需要は、政府による支援プログラムや啓発プログラムにより急増
CAR T細胞療法市場を牽引する主な要因は、がんの罹患率の増加です。PAP(Patient Assistance Program)の利用可能性も、療法の採用を増加させる要因のひとつです。
政府や組織が、がんに関する意識を高めるためのイニシアティブやプログラムを策定しています。こうしたアプローチも市場の成長に貢献しています。例えば、米国がん協会やキャンサーケアなどの組織は、がん治療に伴う困難を乗り越えるための支援を目的としたさまざまなプログラムを提供しています。
- 米国国立がん研究所の最近の報告によると、がんは世界的に主要な死因となっています。2022年には約2000万人が新たにがんと診断され、2024年にはその数が2990万人に達すると予想されています。
- この報告書によると、がんの発生率は男性の方が女性よりも高い。前立腺がん、肺がん、大腸がんなどの発生率は、2024年には男性で約48%に達すると予想されている。
このデータは、CAR T細胞のような効果的なソリューションと、その重要性を周知するための政府の支援の必要性がますます高まっていることを示している。
臨床試験の急増により、高度な治療法のための新たな道筋が生まれる
CAR T細胞療法市場の成長を促すもう一つの重要な要因は、臨床試験の拡大です。これらの試験は、新たな適応症の探索と既存の治療法の改善を目的としています。製薬会社や研究機関は、さまざまな癌を標的とし、患者の転帰を改善する先進的なCAR T細胞療法の開発に向けた研究に投資しています。これには、CAR T細胞の有効性と安全性プロファイルの向上に焦点を当てた試験が含まれます。
CAR T細胞治療と他の治療法を統合した併用療法を調査する研究。臨床試験の増加はCAR T細胞療法の潜在性を裏付けるものであり、利害関係者からの投資や関心を集めています。これは市場のさらなる成長を後押しする要因となります。
市場の抑制要因
CAR T細胞療法のコストの高さが産業用成長の妨げに
CAR T細胞療法の高額な費用は、その普及と利用の大きな障壁となっています。この高額な価格の主な理由のひとつは、複雑で個別化された製造プロセスです。各治療には、患者からT細胞を抽出して遺伝子改変する工程が含まれます。この労働集約的で時間のかかるプロセスが、大幅な費用につながっています。キムリアやイエスカルタなどの一部の療法では、1回の治療につき35万ドルを超えることもよくあります。
米国国立衛生研究所の報告書によると、CAR T細胞療法は最も高額な治療法であり、患者一人当たり37万3000ドルから50万ドル以上の費用がかかっています。この高額な費用により、世界的に市場は変化を迎えています。
治療の厳格な適格基準
CAR T細胞療法の普及におけるもう一つの課題は、すでに広範囲の治療を経験している患者が対象となることです。tisagenlecleucelやaxicabtagene ciloleucelのような治療を受けるには、患者は少なくとも2種類の全身療法を受けている必要があります。
複数の治療を経験した患者の中には、キメラ抗原受容体T細胞治療の重篤な副作用に耐えられるか不安に思う人もいる。この制限により、さらに普及率が低下する。その結果、CAR T細胞療法の厳格な適格基準は、より高い治療費と関連している。この要因は、CAR T療法の普及を妨げる可能性が高い。
- 2021年4月に発行されたMJH Life Sciences誌の記事によると、最近のリアルワールドデータの分析では、CAR T細胞療法の平均総費用は70万ドルを超え、中には100万ドルを超える症例もあることが明らかになった。
主な市場機会
がん治療の研究開発が成長機会を生み出す
肺がん、大腸がん、多発性骨髄腫、前立腺がんなどの癌治療の研究開発への注目が高まっています。この傾向は、CAR T細胞療法の提供者にいくつかの成長機会をもたらすことが予想されます。戦略的買収も、メーカーが市場のより大きなシェア獲得に向けた取り組みを加速するのに役立つ可能性があります。
政府による支援的な政策やライフサイエンスへの資金提供は、近い将来、CAR T細胞療法の需要を促進することが期待されています。例えば、米国では、ライフサイエンス法案により、さまざまな取り組みを支援するために10年間で10億ドルが割り当てられています。
革新的ながん治療法の選択肢に対するニーズの高まりは、キメラ免疫受容体療法市場に関わる人々にとって、大きな収益機会を生み出すことが予想されます。
産業用拡大を加速する治療法の進歩
固形腫瘍への使用は、CAR T細胞療法市場にとって重要な機会であり、治療の成長と進歩を可能にします。
CAR T細胞療法は、B細胞リンパ腫や急性リンパ性白血病(ALL)などの血液がんの治療において大きな成功を収めていますが、固形腫瘍への使用はより困難です。これは主に、固形腫瘍内の厳しい腫瘍微小環境、腫瘍細胞の多様性、物理的障壁などの独特な障害によるものです。これらの課題を克服できれば、市場における新たな成長とイノベーションの機会につながる可能性があります。この分野の企業は、複数の製品と革新的な治療法の開発に取り組んでいます。例えば、
- 米国に拠点を置くスタンフォード・メディスンは、転移性黒色腫の治療に新しい細胞ベースの療法を使用した最初の米国の医療センターとなりました。また、この治療法は固形腫瘍に対してFDAが承認した初の治療法でもあります。この療法は、CAR-T療法と同様に、免疫細胞を使用して癌と戦う能力を高めるものです。
CAR-T細胞療法市場の競合状況
世界的なCAR-T細胞療法市場は、複数の大手企業の存在により、継続的に成長しています。これらの主要企業は、革新的な治療法や治療オプションの導入に重点的に取り組んでいます。
CAR T細胞療法を手掛ける企業は、業界の既存企業や新興企業との提携、規制当局の承認、買収、パートナーシップなどを通じて、市場での存在感を高めるために積極的に取り組んでいます。
また、いくつかの国々の政府も、これらの治療法に対する認知度を高め、開発のための資金調達に貢献しています。2020年には、FDAがマントル細胞リンパ腫患者を対象に、brexucabtagene autoleucel(Tecartus)として知られるCAR T細胞療法を承認しました。
最近の産業用開発
- 2024年4月、インドはがん治療のための同国初の独自開発CAR T細胞療法を発売し、この病気との闘いにおける重要な進歩を遂げた。インド工科大学ボンベイ校とタタ記念センターが開発した遺伝子ベースの療法は、国外の価格の10分の1でインド国内で展開されている。「NexCAR19 CAR T細胞療法」は、治療費を大幅に削減することが期待されている。
- 2024年9月、ムンバイのMOC Cancer Care and Research Centreは、白血病、骨髄腫、リンパ腫などの血液がん患者を対象に、CAR-T細胞療法をサービスに導入しました。この療法は、従来の治療法が効かなくなった患者の治療成績の改善を目的としています。
CAR T細胞療法市場のセグメンテーション
製品別
- Yescarta(axicabtagene ciloleucel)
- Kymriah(tisagenlecleucel)
- JCAR017(lisocabtagene maraleucel)
- bb2121
適応症別
- 再発性大B細胞リンパ腫
- 急性リンパ性白血病(ALL
- 多発性骨髄腫
エンドユーザー別
- 病院でのカーT細胞療法
- がん治療センターでのカーT細胞療法
地域別
- 北米
- ヨーロッパ
- 東アジア
- 南アジアおよび太平洋地域
- 中南米
- 中東およびアフリカ
目次
1. エグゼクティブサマリー
1.1. グローバルCAR T細胞療法市場の概観、2024年と2031年
1.2. 市場機会評価、2024年~2031年、US$ Mn
1.3. 主要な市場動向
1.4. 今後の市場予測
1.5. プレミアム市場洞察
1.6. 業界の動向と主な市場イベント
1.7. PMRの分析と推奨事項
2. 市場概要
2.1. 市場の範囲と定義
2.2. 市場力学
2.2.1. 推進要因
2.2.2. 抑制要因
2.2.3. 機会
2.2.4. 主な傾向
2.3. マクロ経済要因
2.3.1. 世界のセクター別展望
2.3.2. 世界のGDP成長見通し
2.4. COVID-19の影響分析
2.5. 予測要因 – 関連性と影響
3. 付加価値に関する洞察
3.1. 製品採用分析
3.2. 規制環境
3.3. パイプライン分析
3.4. バリューチェーン分析
3.5. PESTLE分析
3.6. ポーターのファイブフォース分析
3.7. 親市場分析
4. 世界のCAR T細胞療法市場の見通し:歴史(2019年~2023年)および予測(2024年~2031年)
4.1. 主なハイライト
4.1.1. 市場規模(US$ Mn)および前年比成長率
4.1.2. 絶対$機会
4.2. 市場規模(US$ Mn)の分析と予測
4.2.1. 市場規模(US$ Mn)の分析(2019年~2022年)
4.2.2. 市場規模(US$ Mn)の分析と予測(2023年~2031年)
4.3. 世界のCAR T細胞療法市場の見通し:製品
4.3.1. はじめに / 主な調査結果
4.3.2. 製品別、2019年~2022年の市場規模(US$ Mn)の推移
4.3.3. 製品別、2023年~2031年の市場規模(US$ Mn)の推移と予測
4.3.3.1. Yescarta(axicabtagene ciloleucel)
4.3.3.2. Kymriah(tisagenlecleucel)
4.3.3.3. JCAR017(lisocabtagene maraleucel)
4.3.3.4. bb2121
4.3.4. 市場の魅力分析:製品
4.4. 世界のCAR T細胞療法市場の見通し:適応症
4.4.1. はじめに/主な調査結果
4.4.2. 適応症別市場規模推移(単位:百万米ドル)分析、2019年~2022年
4.4.3. 適応症別:現在の市場規模(百万米ドル)の分析と予測、2023年~2031年
4.4.3.1. 再発性大B細胞リンパ腫
4.4.3.2. 急性リンパ性白血病(ALL)
4.4.3.3. 多発性骨髄腫
4.4.4. 市場の魅力分析:適応症
4.5. 世界のCAR T細胞療法市場の見通し:エンドユーザー
4.5.1. はじめに/主な調査結果
4.5.2. エンドユーザー別、2019年~2022年の市場規模(米ドル百万)の推移
4.5.3. 現在の市場規模(US$ Mn)分析および予測、エンドユーザー別、2023年~2031年
4.5.3.1. 病院におけるCAR T細胞療法
4.5.3.2. がん治療センターにおけるCAR T細胞療法
4.5.4. 市場魅力度分析:エンドユーザー
5. 世界のCAR T細胞療法市場の見通し:地域
5.1. 主なハイライト
5.2. 地域別市場規模(百万米ドル)の推移分析、2019年~2022年
5.3. 地域別市場規模(百万米ドル)の現状分析と予測、2023年~2031年
5.3.1. 北米
5.3.2. 欧州
5.3.3. 東アジア
5.3.4. 南アジアおよびオセアニア
5.3.5. ラテンアメリカ
5.3.6. 中東およびアフリカ
5.4. 市場魅力度分析:地域
6. 北米CAR T細胞療法市場の見通し:2019年~2023年の実績および2024年~2031年の予測
6.1. 主なハイライト
6.2. 市場別、2019年~2022年の市場規模(US$ Mn)の分析
6.2.1. 国別
6.2.2. 製品別
6.2.3. 適応症別
6.2.4. エンドユーザー別
6.3. 国別、2023年から2031年の現在の市場規模(百万米ドル)の分析と予測
6.3.1. 米国
6.3.2. カナダ
6.4. 製品別、2023年から2031年の現在の市場規模(百万米ドル)の分析と予測
6.4.1. Yescarta(axicabtagene ciloleucel)
6.4.2. Kymriah(tisagenlecleucel)
6.4.3. JCAR017(lisocabtagene maraleucel)
6.4.4. bb2121
6.5. 適応症別、2023年から2031年の現在の市場規模(百万米ドル)の分析と予測
6.5.1. 再発性大B細胞リンパ腫
6.5.2. 急性リンパ性白血病(ALL)
6.5.3. 多発性骨髄腫
6.6. 現在の市場規模(百万米ドル)の分析と予測、エンドユーザー別、2023年~2031年
6.6.1. 病院におけるCAR T細胞療法
6.6.2. がん治療センターにおけるCAR T細胞療法
6.7. 市場魅力度分析
7. 欧州CAR T細胞療法市場の見通し:2019年~2023年の実績および2024年~2031年の予測
7.1. 主なハイライト
7.2. 市場別、2019年~2022年の実績市場規模(US$ Mn)分析
7.2.1. 国別
7.2.2. 製品別
7.2.3. 適応症別
7.2.4. エンドユーザー別
7.3. 現在の市場規模(US$ Mn)の分析と予測、国別、2023年~2031年
7.3.1. ドイツ
7.3.2. フランス
7.3.3. 英国
7.3.4. イタリア
7.3.5. スペイン
7.3.6. ロシア
7.3.7. トルコ
7.3.8. その他の欧州
7.4. 製品別 市場規模(百万米ドル)分析と予測、2023年~2031年
7.4.1. Yescarta(axicabtagene ciloleucel
7.4.2. Kymriah (tisagenlecleucel)
7.4.3. JCAR017 (lisocabtagene maraleucel)
7.4.4. bb2121
7.5. 適応症別市場規模(US$ Mn)分析と予測、2023年~2031年
7.5.1. 再発性大B細胞リンパ腫
7.5.2. 急性リンパ芽球性白血病(ALL)
7.5.3. 多発性骨髄腫
7.6. 現在の市場規模(百万米ドル)分析と予測、エンドユーザー別、2023年~2031年
7.6.1. 病院におけるCAR T細胞療法
7.6.2. がん治療センターにおけるT細胞療法
7.7. 市場魅力度分析
8. 東アジアCAR T細胞療法市場の見通し:2019年~2023年の実績および2024年~2031年の予測
8.1. 主なハイライト
8.2. 市場別、2019年~2022年の市場規模(US$ Mn)の分析
8.2.1. 国別
8.2.2. 製品別
8.2.3. 適応症別
8.2.4. エンドユーザー別
8.3. 国別、2023年から2031年の現在の市場規模(百万米ドル)の分析と予測
8.3.1. 中国
8.3.2. 日本
8.3.3. 韓国
8.4. 製品別、2023年から2031年の現在の市場規模(百万米ドル)の分析と予測
8.4.1. Yescarta(axicabtagene ciloleucel)
8.4.2. Kymriah(tisagenlecleucel)
8.4.3. JCAR017(lisocabtagene maraleucel)
8.4.4. bb2121
8.5. 適応症別、2023年から2031年の現在の市場規模(US$ Mn)の分析と予測
8.5.1. 再発性大B細胞リンパ腫
8.5.2. 急性リンパ性白血病(ALL)
8.5.3. 多発性骨髄腫
8.6. 現在の市場規模(百万米ドル)の分析と予測、エンドユーザー別、2023年~2031年
8.6.1. 病院におけるCAR-T細胞療法
8.6.2. がん治療センターにおけるCAR-T細胞療法
8.7. 市場の魅力分析
9. 南アジアおよびオセアニアCAR T細胞療法市場の見通し:2019年~2023年の実績および2024年~2031年の予測
9.1. 主なハイライト
9.2. 市場別、2019年~2022年の実績市場規模(US$ Mn)分析
9.2.1. 国別
9.2.2. 製品別
9.2.3. 適応症別
9.2.4. エンドユーザー別
9.3. 現在の市場規模(US$ Mn)分析および予測、国別、2023年~2031年
9.3.1. インド
9.3.2. 東南アジア
9.3.3. ANZ
9.3.4. 南アジアおよびオセアニアのその他
9.4. 製品別 市場規模(US$ Mn)分析および予測、2023年~2031年
9.4.1. Yescarta(axicabtagene ciloleucel
9.4.2. Kymriah(tisagenlecleucel
9.4.3. JCAR017(lisocabtagene maraleucel)
9.4.4. bb2121
9.5. 適応症別、2023年から2031年の現在の市場規模(US$ Mn)の分析と予測
9.5.1. 再発性大B細胞リンパ腫
9.5.2. 急性リンパ性白血病(ALL)
9.5.3. 多発性骨髄腫
9.6. 現在の市場規模(US$ Mn)分析と予測、エンドユーザー別、2023年~2031年
9.6.1. 病院におけるCAR T細胞療法
9.6.2. がん治療センターにおけるCAR T細胞療法
9.7. 市場魅力度分析
10. ラテンアメリカCAR T細胞療法市場の見通し:2019年~2023年の過去実績と2024年~2031年の予測
10.1. 主なハイライト
10.2. 市場別、2019年~2022年の過去市場規模(US$ Mn)分析
10.2.1. 国別
10.2.2. 製品別
10.2.3. 適応症別
10.2.4. エンドユーザー別
10.3. 現在の市場規模(US$ Mn)分析および予測、国別、2023年~2031年
10.3.1. ブラジル
10.3.2. メキシコ
10.3.3. その他のラテンアメリカ
10.4. 製品別現在の市場規模(US$ Mn)分析と予測、2023年~2031年
10.4.1. Yescarta(axicabtagene ciloleucel
10.4.2. Kymriah(tisagenlecleucel
10.4.3. JCAR017(lisocabtagene maraleucel)
10.4.4. bb2121
10.5. 適応症別、2023年から2031年の現在の市場規模(US$ Mn)の分析と予測
10.5.1. 再発性大B細胞リンパ腫
10.5.2. 急性リンパ芽球性白血病(ALL)
10.5.3. 多発性骨髄腫
10.6. 現在の市場規模(US$ Mn)分析と予測、エンドユーザー別、2023年~2031年
10.6.1. 病院におけるCAR T細胞療法
10.6.2. がん治療センターにおけるCAR T細胞療法
10.7. 市場魅力度分析
11. 中東およびアフリカのCAR T細胞療法市場の見通し:2019年~2023年の過去実績および2024年~2031年の予測
11.1. 主なハイライト
11.2. 市場別、2019年~2022年の過去市場規模(US$ Mn)分析
11.2.1. 国別
11.2.2. 製品別
11.2.3. 適応症別
11.2.4. エンドユーザー別
11.3. 現在の市場規模(US$ Mn)分析と予測、国別、2023年~2031年
11.3.1. GCC諸国
11.3.2. エジプト
11.3.3. 南アフリカ
11.3.4. 北アフリカ
11.3.5. 中東およびアフリカのその他
11.4. 製品別市場規模(US$ Mn)分析と予測、2023年~2031年
11.4.1. Yescarta(axicabtagene ciloleucel
11.4.2. Kymriah (tisagenlecleucel)
11.4.3. JCAR017 (lisocabtagene maraleucel)
11.4.4. bb2121
11.5. 適応症別市場規模(US$ Mn)分析と予測、2023年~2031年
11.5.1. 再発性大B細胞リンパ腫
11.5.2. 急性リンパ性白血病(ALL)
11.5.3. 多発性骨髄腫
11.6. 現在の市場規模(US$ Mn)分析と予測、エンドユーザー別、2023年~2031年
11.6.1. 病院におけるT細胞療法
11.6.2. がん治療センターにおけるT細胞カー・セラピー
11.7. 市場魅力度分析
12. 競合状況
12.1. 市場シェア分析、2023年
12.2. 市場構造
12.2.1. 市場ごとの競合状況マッピング
12.2.2. 競合ダッシュボード
12.3. 企業プロファイル(詳細情報 – 概要、財務状況、戦略、最近の動向)
*** 本調査レポートに関するお問い合わせ ***
