世界の医療規制関連業務アウトソーシング市場(2024年~2032年):サービス別、その他

※本ページに記載されている内容は英文レポートの概要と目次を日本語に自動翻訳したものです。英文レポートの情報と購入方法はお問い合わせください。
*** 本調査レポートに関するお問い合わせ ***
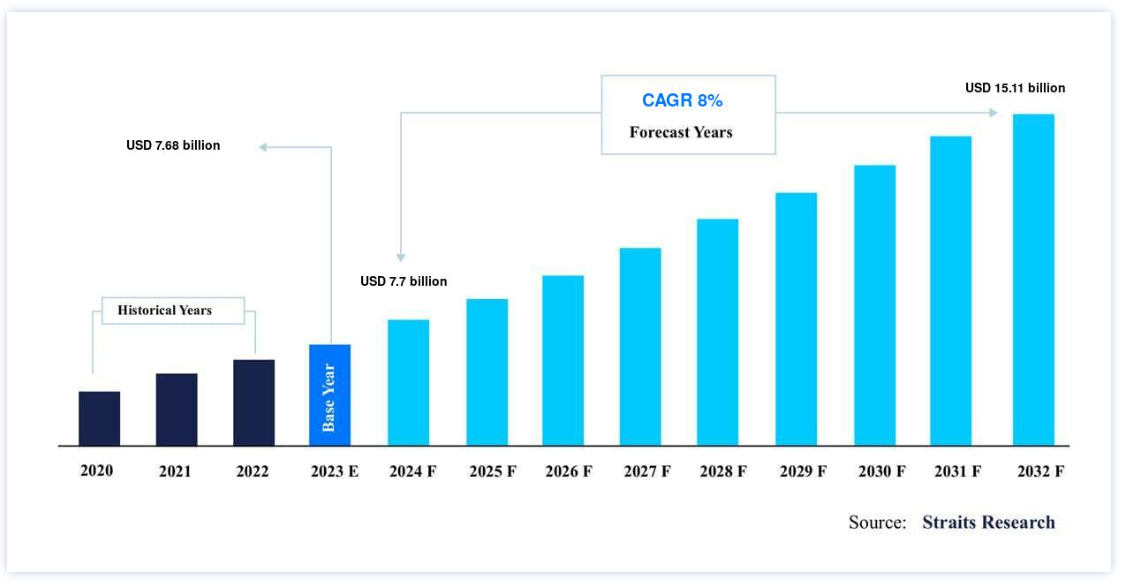
世界の医療規制関連業務アウトソーシング市場規模は、2023年に76.8億米ドルと評価され、予測期間中(2024-2032年)にCAGR 8%を記録し、2032年までに151.1億米ドルに達すると予測されています。
予測期間中の市場シェアの増加は、医療規制の複雑化とコンプライアンスを確保するための専門知識の必要性に関連しており、これが薬事アウトソーシングサービスの需要を促進しています
医療薬事アウトソーシングとは、薬事業務を専門のサービスプロバイダーに委託することである。 これには、製品登録、臨床試験承認、ラベリングコンプライアンス、ファーマコビジランス、市販後モニタリングなどが含まれる。 アウトソーシングは製薬業界やバイオテクノロジー業界で広く普及しており、製造コストの削減や新技術の活用を可能にしている。 規制の枠組みが複雑かつ変化していること、医薬品研究活動が活発化していること、コスト効率が重視されていることなどから、市場は近年劇的に拡大している;
アウトソーシングサービスは、企業が複雑な規制の枠組みを理解し、コンプライアンスを確保し、規制当局とのシームレスなコンタクトを促進するのを支援する。 その目的は、合理化された承認プロセスと規制コンプライアンスを提供することである。 薬事業務を専門機関にアウトソーシングする企業は、プロセスの合理化、コンプライアンスの向上、ヘルスケア製品の承認の迅速化を実現し、最終的には世界的な事業拡大計画や市場参入を成功させることができます。 製薬、バイオテクノロジー、医療機器の各企業は、薬事業務を専門企業にアウトソーシングすることで、複雑な規制の枠組みをより効率的に進め、変化する基準に確実に対応し、規制要件を満たしたヘルスケア製品の承認と販売を迅速化することができます。
トップ2 主要ハイライト
サービス別では、製品登録と臨床試験アプリケーションが市場をリード
エンドユーザー別では、医薬品が市場をリードしている。
世界の医療薬事アウトソーシング市場の成長要因
規制当局による厳しい規制
先進国および発展途上国における医療分野への投資の増加、医薬品開発企業と規制当局のアウトソーシング企業との協力関係の強化が市場成長の原動力。 研究開発活動の増加と特許失効が市場成長の原動力となっている。 世界的に、医薬品や機器の製造に関する文書化に対する規制圧力の高まりが、医療薬事アウトソーシングの需要を後押ししている;
さらに、規制当局が課す厳しい規制により、中小企業は登録、評価、規制に準拠した文書の作成に対応できる訓練された熟練した薬事専門家を雇用せざるを得なくなり、市場の成長をさらに後押ししています。 このような背景から、企業が規制要件を効果的に満たし、規制基準の遵守を維持しながら医療用医薬品の承認と上市を迅速に行う上で、アウトソーシングが重要な役割を担っていることが浮き彫りになっている。
迅速な製品承認への需要の高まり
医療規制関連業務アウトソーシング市場の最も顕著な促進要因は、最小限の運用コストで新製品を承認する必要性が高まっていることである。 医療規制当局の承認プロセスは厳格化し、時間がかかるようになっているため、市場関係者は競争優位性を獲得するため、最初の試みで製品承認を取得しようと努力している。 厳しい規制と発展途上国における規制状況の変化により、企業は社内に薬事部門を設置するか、薬事業務をアウトソーシングする必要に迫られている
また、薬事情報システムに対する投資が増加し、薬事出版やオペレーションなどの業務を自動化していることも、市場成長の原動力となっている。 この傾向は、製品の迅速な承認取得と上市にアウトソーシングが不可欠であることを示している。 アウトソーシングは世界的な成長努力の成功に貢献し、医療業界がすべてのルールに従うことを保証する。
市場抑制要因
アウトソーシングのリスク
医療法務をアウトソーシングすることによるリスクは、市場の成長を鈍らせる可能性がある。 こうしたリスクの中には、アウトソーシング先が製薬事業に関する個人データにアクセスできる可能性があり、プライバシーやコンプライアンスが損なわれる可能性があるため、データの共有やセキュリティに関するものがある。 また、COVID-19のパンデミックのような事象の影響も受け、臨床研究や規制活動が一時的に停止し、市場のあり方に悪影響を及ぼしている。
複雑な規制環境
医療ビジネスは、常に新しい規則や基準が発表され、常に変化する規制環境の中で行われています。 規制はより複雑化し、より詳細な指示やコンプライアンス要件があるため、企業はルールに従うための支援を必要としています。 このことは、複雑な規則を理解し遵守するために、外部の規制問題の専門家を雇うことの重要性を示している。 こうすることで、品質やコンプライアンスを犠牲にすることなく、コンプライアンスを確保し、変化する規制環境に対応することができる。
市場機会
研究開発費の増加
医療薬事アウトソーシング市場には、研究開発費の増加、臨床試験数の増加、アウトソーシングの費用対効果など、さまざまな要因の機会があります。 これらの変数は、ヘルスケアにおける薬事アウトソーシングサービスの必要性に大きく影響します。 研究開発費の増加は、技術革新へのコミットメントと斬新なヘルスケア商品の創造を示しており、これらの商品を迅速に市場に投入するための効果的な規制プロセスを要求している;
さらに、臨床試験の世界的な増加は、複雑な規制の枠組みを横断し、変化する要件へのコンプライアンスを維持するための専門的な薬事スキルの必要性を浮き彫りにしている。 薬事業務のアウトソーシングは費用対効果に優れているため、企業はリソースを最大限に活用し、コアコンピタンスに集中することができ、社内の薬事担当者に関連する管理コストを負担することなく、専門的な薬事知識を得ることができる
地域別インサイト
北米: 市場シェア7.6%で圧倒的な地域
北米が最も大きな市場シェアを占めており、予測期間中の年平均成長率は7.6%と推定される。 北米における医療薬事アウトソーシングサービスの成長は、大手製薬企業による薬事業務のアウトソーシングが牽引しており、これは償還シナリオの変化やジェネリック医薬品の競争、価格圧力などの結果である。 さらに、研究開発活動の活発化と臨床試験の増加により、同地域の市場は成長を遂げるだろう。 例えば、Global Observatory on Health R&Dによると、米国は2021年に10,870件の臨床試験を登録し、全体の18.1%を占める。 カナダは2021年に2,099件の臨床試験を登録し、全体の3.5%を占めた。 その結果、薬事アウトソーシング市場は、同地域で実施される数多くの臨床試験によって牽引されると予想される。
さらに、市場の拡大は戦略的パートナーシップや地域の有力な競合企業によって促進されている。 例えば、2021年4月、ParexelとVeeva Systemsは、テクノロジーとプロセスイノベーションの活用による臨床試験の迅速化を目的とした戦略的提携を発表した。 各事業の薬事コンサルティングサービスは、他方にとって有利なものとなる。
ヨーロッパ 年平均成長率が最も高い急成長地域
欧州は予測期間中、年平均成長率8.2%で成長すると推定される。 ドイツ、英国、フランスといった国々がリードしているのは、強力な医療制度と厳格な規則があるからである。 この地域は、多くの臨床研究グループがあり、医療に多くの資金を費やし、研究開発に力を入れ、新技術を使用していることから利益を得ている。 ヨーロッパには2つの新市場がある。 ドイツが最も大きなシェアを占めている。 こうした要因から、欧州は医療薬事アウトソーシング市場で高いシェアを占めている。
アジア太平洋地域が最も急速に成長すると予想される。 これは、より多くの医薬品が製造され、政府がビジネスをしやすくしており、特に中国とインドでは人々の医療への支出が増えているためである。 製薬会社やバイオテクノロジー企業は、研究開発への投資を増やし、より多くの臨床試験を実施し、薬事承認をアウトソーシングしている。 これらはすべて、この地域の成長を支えている。 アジア太平洋市場では臨床試験の申請が多く、薬事アウトソーシングサービスの需要を促進する上で、この地域がいかに重要であるかを示している。
中東とアフリカの市場は他と比べると小さいが、より多くの製薬会社が進出しており、医療インフラも改善されているため、市場は拡大している。
医療薬事アウトソーシング市場のセグメント分析
サービス別
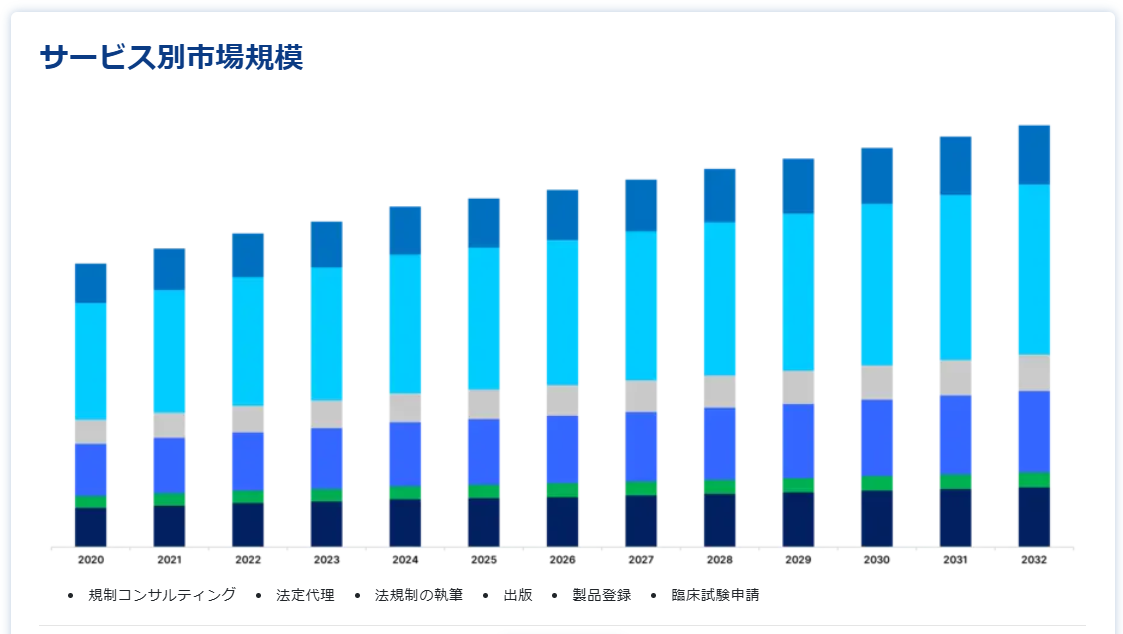
市場はさらに、薬事コンサルティング、法務代理、薬事関連の執筆・出版、製品登録、臨床試験申請に区分される。 市場シェアが最も高いのは製品登録と臨床試験申請である。 製品登録および臨床試験アプリケーションの優位性は、臨床試験の世界的な増加、既存市場における厳しい規制、アジア太平洋地域などの新興地域における法規制改革に起因している。 この分野は、ヘルスケア商品の承認・登録を促進し、規制遵守を保証し、製薬、バイオテクノロジー、医療機器メーカーの市場参入を加速する上で極めて重要である。 臨床試験サービスに対するニーズの高まりと効果的な製品登録プロセスの必要性が、医療薬事アウトソーシング市場におけるこの分野の重要性を高めている。
一方、薬事関連の文書作成と出版は、薬事コンプライアンスに必要な薬事関連の文書、提出書類、出版物を作成することから、大きな市場シェアを占めている。 この分野は、正確で綿密な薬事関連文書の作成、規制当局との効果的な連携、製品開発・承認プロセス全体を通しての薬事コンプライアンスの保証など、企業を支援するものである。 その結果、臨床試験管理および製品登録における極めて重要な役割により、製品登録および臨床試験アプリケーション部門が市場シェアをリードしている。 対照的に、薬事関連文書作成・出版分野は、薬事関連文書作成と規制当局とのコミュニケーションにおいて企業を支援することで僅差で続いている。
エンドユーザー別
市場はさらに医療機器、医薬品、バイオテクノロジー、食品・飲料に区分される。 医薬品ビジネスが市場で大きな位置を占めているのは、医薬品の製造、承認、販売方法について多くの規則が存在するからである。 製薬会社は、複雑な薬事規制の状況に対応し、厳格な規則を守り、新薬や治療法の承認取得までのプロセスをスピードアップするために、薬事業務のアウトソーシングに依存しています。 製薬業界がアウトソーシングサービスを必要としているのは、規制に関する事柄が非常に重要だからです。 そのため、製薬業界は市場の主要なエンドユーザーとなっている。
医療機器業界は、医薬品業界に次いで重要なエンドユーザーグループである。 規制上の問題は、製薬会社に影響を与えるのと同じように、医療機器会社にも影響を与えます。 これらの企業は、承認を取得し、薬事規制の経路をナビゲートし、変化する基準へのコンプライアンスを確保するために、専門的な知識を必要とします。 薬事業務をアウトソーシングすることで、医療機器メーカーは新しいアイデアや製品開発に集中できる一方、外部の薬事専門家を利用して薬事プロセスを迅速化し、顧客が製品を入手しやすくすることができる。
医療薬事アウトソーシング市場のセグメンテーション
サービス別(2020年〜2032年)
規制コンサルティング
法定代理
法規制の執筆
出版
製品登録
臨床試験アプリケーション
エンドユーザー別 (2020-2032)
医療機器
医薬品
バイオテクノロジー
食品と飲料
 目次
目次
1. エグゼクティブサマリー
2. 調査範囲とセグメンテーション
3. 市場機会の評価
4. 市場動向
5. 市場の評価
6. 規制の枠組み
7. ESGの動向
8. 世界の医療規制関連業務アウトソーシング市場規模分析
9. 北米の医療規制関連業務アウトソーシング市場分析
10. ヨーロッパの医療規制関連業務アウトソーシング市場分析
11. APACの医療規制関連業務アウトソーシング市場分析
12. 中東・アフリカの医療規制関連業務アウトソーシング市場分析
13. ラタムの医療規制関連業務アウトソーシング市場分析
14. 競合情勢
15. 市場プレイヤーの評価
16. 調査方法
17. 付録
18. 免責事項
*** 本調査レポートに関するお問い合わせ ***
